

酒石酸溴莫尼定滴眼液
沐利汀® BRIMOCON®
Brimonidine Tartrate Eye Drops
Jiu Shi Suan Xiu Mo Ni Ding Di Yan Ye
活性成分:酒石酸溴莫尼定。
化学名称:5-溴-6-(2-咪唑双烯氨)喹噁啉 L-酒石酸
化学结构式: 
分子式:C11H10BrN5•C4H6O6
分子量:442.24
防腐剂:苯扎氯铵 0.005%
本品为淡黄色或淡黄绿色澄明液体。
本品适用于降低开角型青光眼和高眼压症患者的眼压。部分患者长期使用本品时,其降低眼压的作用逐渐减弱。作用减弱出现的时间因人而异,因此应予以密切关注。
5ml:10mg
滴入眼睑内,常规剂量滴入患者眼每日2次,每次1滴。眼压峰值在下午或眼压需额外控制的患者,下午可增加 1滴。本品可与其它局部滴眼液联合使用。同时使用不止一种滴眼液时,每种药物的滴眼时间至少间隔 5 分钟。
在溴莫尼定滴眼液临床研究期间报告了以下不良反应,并按照以下惯例分类:非常常见(≥1/10),常见(≥1/100至<1/10),不常见(≥1/1,000至<1/100),罕见(≥1/10,000 至<1/1,000)和非常罕见(<1/10,000)。在每个频率组内,按严重性降序呈列了不良反应。
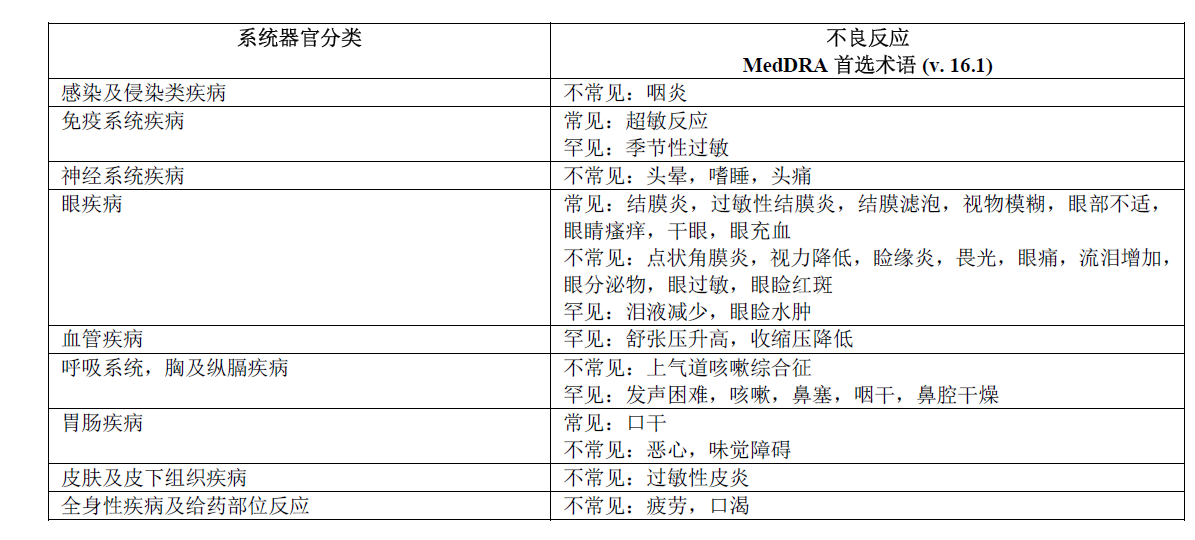
通过上市后监测确定的溴莫尼定滴眼液的不良反应还包括以下几项。不能从可用数据中估计频率。在每个系统器官分类内,按严重性降序列示不良反应。

本品禁用于对酒石酸溴尼定或本品中任何成份过敏者,亦禁用于使用单胺氯化抑制剂治疗的患者。
1.尽管临床研究中本品对患者的血压影响甚小,但有严重心血管疾患的患者使用的仍应谨慎。
2.由于未进行肝或肾功能受损患者使用本品的研究,故在治疗此类患者时,应谨慎。
3.精神抑郁,大脑或冠状动脉机动不,雷诺氏现象,直立性低血压,血栓闭塞性脉管炎的患者,使用本品均谨慎。
4.研究期间某些患者使用本品的作用减弱,使用酒石酸莫尼定滴眼液治疗时,在第一个月观察到降眼压未必都能反映长期降眼压的水平,对使用降眼压药的患者,应按常规期监测眼内压。
5.本品中使用的保存剂为苯扎氯铵,而苯扎氯铵有可能被软性接触镜,困此应向配戴软性接触镜的患者说明,在滴用本品后至少等待15分钟再配戴。
6.与各种α—肾上腺素能受体激动剂一样,本品亦可使某些患者产生疲劳和/或倦怠,因此应提醒从事危险作业的患者使用本品有出现精神集中下降的可能性。
7.酒石酸溴莫尼定可能会引起眼部过敏反应。如果患者出现过敏反应,应停止治疗。
8.已报告使用酒石酸溴莫尼定时出现了迟发性眼部超敏反应,有些报告称与 IOP 升高相关。
孕妇用药:
未进行孕妇使用本品的研究,但在动物研究中有极少量的溴莫尼定可通过胎盘, 进入胎鼠的循环系统。因此只有判定本品可能给母亲带来的利益大于给胎儿带来的潜在危险时,方可使用。
哺乳期妇女用药:
虽然在动物试验中已发现酒石酸溴莫尼定随乳汁排出,但在人体中本品是否亦随母乳排出,尚不明确。因此是否终止授乳或停止用药,应视本品对哺乳期妇女的重要性而定。
在儿科青光眼患者(2-7 岁)进行的临床试验中,使用 0.2%酒石酸溴莫尼定滴眼液毎日 3次最常见的不良反应为嗜睡(50%-83%的患者年龄为 2-6 岁)和警惕性降低。在 7岁或 7岁以上的儿科患者中(>20kg),嗜睡发生的频率比较低(25%)。由于最常见的不良反应是嗜睡,因此有约 16%的患者由于使用 0.2%酒石酸溴莫尼定滴眼液出现嗜睡而中断了试验。
在低于 2岁的儿科患者中,还未进行 0.2%酒石酸溴莫尼定滴眼液的安全性和有效性研究,因此建议低于 2岁的儿科患者不宜使用 0.2%酒石酸溴莫尼定滴眼液。(也请参照不良反应章节)
年龄较大患者(65岁以上患者)单剂量使用溴莫尼定后的 Cmax、AUC 以及半衰期与年轻人相同,表明溴莫尼定的全身吸收和消除不受年龄影响。包括年龄较大患者参加的为期 3 个月临床研究的数据显示,溴莫尼定对全身的影响非常小。
1.禁用于正在使用单胺氧化酶抑制剂的患者。
2.建议正在使用可影响去甲肾上腺素能传输的抗抑郁药(例如,三环类抗抑郁药和米安色林)的患者应慎用。此外,已报告称三环类抗抑郁药使系统性可乐定的降压作用减弱。目前没有与给药后循环中的儿茶酚胺类药物的水平有关的数据。然而,建议正在使用会影响循环中的胺类代谢和摄取的药物(例如,氯丙嗪,哌醋甲酯,利血平)的患者慎用。
3.α受体激动剂为一类可降低脉率和血压的药物。与抗高血压药和/或具有类似心血管效应(引起低血压的药物)的强心苷类药物伴随使用时要慎重。
4.使用CNS抑制剂(例如,乙醇,巴比妥类,阿片类,镇静剂或麻醉剂)时应考虑出现累加效应或增强效应这种可能性。
5.在开始全身性(无论何种剂型)伴随使用(或更改剂量时)可能会与α-肾上腺素能受体激动剂相互作用或干扰其活性的药物时(即,肾上腺素能受体激动剂或拮抗剂,例如,异丙肾上腺素,哌唑嗪)要慎重。
意外摄入导致的系统性过量(成人):
成人意外摄入溴莫尼定的相关信息非常有限。
口服本品过量时可采用支持疗法或对症治疗;应保持患者呼吸道畅通。
已报告称其他α-2受体激动剂口服过量引起了低血压,乏力,呕吐,昏睡,镇静,心动过缓,心律失常,瞳孔缩小,呼吸暂停,眼压过低,体温过低,呼吸抑制和癫痫发作之类的症状。
儿科人群:
已发表或报告儿科受试者不慎食入本品以后出现了严重副作用。受试者出现了 CNS 抑制症状,通常为暂时昏迷或意识水平低,昏睡,嗜睡,眼压过低,心动过缓,体温过低,苍白,呼吸抑制和呼吸暂停,需送入重症监护室进行护理,如有指征可插管。报告显示所有受试者都已完全痊愈,通常在 6-24 个小时之内痊愈。
眼压升高是造成青光眼视野缺损的主要危险因素。眼压越高,视神经受损和视野缺损的可能性也就越大。酒石酸溴莫尼定有降低眼压的作用,而对心血管和肺功能的影响很小。
在多项长达一年与 0.5%的噻吗心安对比的临床研究中,酒石酸溴莫尼定滴眼液降低眼压幅度约为4~6mmHg,噻吗心安约 6mmHg。因未能适当地控制眼压而退出研究的受试者占 8%,其中 30%发生在治疗第一个月。因各种不良反应而未继续用药者约占 20%。
药理作用:
酒石酸溴莫尼定为肾上腺素能α受体激动剂,本品用药后两小时降眼压效果达到高峰。在动物及人体中用荧光光度测定法进行的研究表明,酒石酸溴莫尼定具有双重的作用机制:既减少房水的生成,又增加葡萄膜巩膜的房水外流。
毒理研究:
致癌性:在小鼠和大鼠每日分别口服 2.5mg/kg和 1.0mg/kg 剂量(按推荐的滴 眼剂量计,分别约为人血浆中本品的 77倍和 118倍),为期 21 个月和 2 年的研究观察中,均未见与药物有关的致癌作用。
遗传毒性:Ames 试验、中国仓鼠卵巢(CHO)细胞染色体畸变试验、小鼠促细胞发生的研究以及显性致死分析中,未见本品的致突变作用。
生殖毒性:大鼠口服溴莫尼定 0.66mg/kg,未见对胎鼠的损害。此剂量相当于给人多次滴眼后人血浆中药物浓度的 100 倍。
眼部给予 0.2%滴眼液后,血浆浓度于 1~4 小时内达到峰值,然后下降,全身的半衰期约为 3小时。
在人体中,溴莫尼定的全身代谢是广泛的。主要代谢部位为肝脏。原形药物及其代谢物主要经尿排泄。口服放射性标记的溴莫尼定后,约 87%的药物在 120小 时内被清除,尿中约占 74%。
置于 15-25℃保存。
5ml无菌滴眼液,置于DROPTAINER ® 塑料滴瓶中。1支/盒。
24个月
进口药品注册标准:JX20110210
进口药品注册证号:H20150504
FDA妊娠分级:B